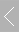在这篇综述中,我们探讨了维生素D与成岩风险之间的关系,并提出了需要对骨骼健康进行药物干预的成石剂的替代方案。最近的国家健康和营养检查调查报告称,自1980年以来,美国肾结石的患病率几乎增加了两倍。结石的终生患病率目前为 8.8%,在男性中更为普遍,尽管女性正在缩小这一差距。1钙结石是迄今为止最常见的结石类型,占所有结石的85%以上。2肾结石与体重指数增加、体重增加、糖尿病、1以及富含动物蛋白和钠的饮食,而它们与液体摄入量,钾和膳食钙成反比。2尿钙排泄量高是肾结石的重要危险因素,与骨密度低 (BMD) 相关3和骨折。
考虑到肠道对钙的吸收导致结石形成剂中钙质的很大一部分,5从理论上讲,补充维生素D可能会增加肠道吸收和岩性生成。最近的多个方面数据显示,在一般人群中,补充维生素D不会有肾结石的风险。6然而,摄入维生素 D或血清水平升高是否会导致已知结石形成者或遗传易感亚组结石仍然是一个悬而未决的问题。维生素D缺乏症与多种疾病有关,因此,随之而来的是测试和处方的激增。7频繁补充维生素D与肾结石患病率较高之间的重叠导致了对因果关系的探索。这样的一个问题很重要,因为筛查维生素D并补充维生素D以响应低值的好处似乎没什么好处,即使在BMD降低的人中也是如此。
钙结石形成是一个复杂的生理过程,通过多个所谓的机制模型进行了广泛的研究,其细节超出了本综述的范围。虽然仍有许多未知之处,但结石形成的广泛先决条件是更高的过饱和度,结晶,生长和聚集。尿液的复杂化学性质,如pH值,多离子含量,启动子浓度和抑制剂都有助于。钙结石形成剂中常见的尿路异常是尿钙排泄量较高,其解释往往未被发现。据说这些患者有特发性钙结石。遗传因素无疑是重要的,但相关的基因并不能完全解释显着遗传性的证据。
由于大多数结石由钙组成,因此其代谢和控制的饮食机制非常令人感兴趣。重要的是,钙限制不会减少结石的形成。事实上,限制膳食钙会增加产石性尿液因子,并可能会引起骨骼脱矿质,2一种在成石剂中发现的现象更明显,即维生素D不足风险增加的人群,8骨密度下降和骨折。4Curhan等人在一项大型前瞻性研究中发现,膳食钙摄入量和肾结石的风险呈负比。2作者提出,钙摄入与膳食草酸盐结合,减少其被肠道吸收并随后在尿液中排泄。另一方面,钙补充剂与结石风险增加有关。未能在膳食草酸盐的同时给予口服钙补充剂可能会为这种差异提供解释。使用钙补充剂的配方可能会有影响,因为柠檬酸钙可能比碳酸钙的岩石性低。9维生素D是钙稳态和骨代谢中不可或缺的一部分,其补充在结石成形剂和非结石成形剂中一直是骨密度,必要性,安全性和功效方面存在一些争议的话题。
维生素D是一种脂溶性维生素,其天然形式不活跃,主要从皮肤中阳光刺激的合成中获得,而从饮食中获得较少。维生素D在肝脏中通过25-羟化酶(CYP2PR1)羟基化,产生25-羟基维生素D3.随后的羟基化,主要是在肾脏中,通过1α-羟化酶(CYP27B1)导致生物活性形式1,25-二羟基维生素D的产生3(骨化三醇)。骨化三醇与靶组织中的细胞内受体结合,促进各种相关基因的转录。骨化三醇的基本功能是促进肠道钙的吸收。然而,它也直接抑制甲状旁腺激素(PTH)的释放,促进肾脏和肠道磷酸盐的吸收,并调节成骨细胞功能和骨吸收。3到钙化酸(图1)。它还作用于前体25-羟基维生素D3,在几种负反馈机制的控制下,防止其转换为活性形式。这种失活酶(将在下面详细讨论)可能在肾钙质沉着症和肾结石患者中起关键作用,特别是在补充维生素D的情况下。
图 1.维生素D的代谢途径以及激活和抑制因子。(1α-OHase, 1α-羟化酶; 24,25-(OH)2D3,24,25-二羟基胆钙化醇)。
由于维生素D直接刺激肠道钙的吸收,因此已被广泛研究以确定升高的水平是否增加尿钙排泄并有助于钙结石的形成。在前瞻性随访的男性和女性队列中,未选择的结石形成剂中的骨化三醇水平升高,并且与肾结石风险较高独立相关。血清钙和PTH不是。11此外,酮康唑是维生素 D 合成的有效抑制剂(通过 1α-羟化酶,CYP27B1),(图 1)有效地降低了一些尿钙排泄量较高的患者的血清骨化三醇和尿钙。12虽然正常个体的尿钙随肠道吸收成比例地增加,但尿钙排泄较高的患者在任何肠道吸收水平上都显示出夸张的钙反应。此外,与非结石成形剂相比,钙结石成形剂的尿钙含量更高,无论从饮食中摄入多少钙。5很明显,虽然维生素D能增加肠道对钙的摄取,但除了纯肠道过度吸收之外,可能还有别的增加钙的机制。
尽管有上述数据,但由于严格的调节机制,补充维生素D对肠道钙吸收和尿钙排泄的刺激并不是不可避免的。1α-羟化酶(CYP27B1,激活酶)的基因转录和酶活性均通过PTH,低血清钙和磷酸盐上调,并通过1,25-二羟基维生素D下调3.此外,CYP24A1(失活酶)通过种种遗传和表观遗传机制上调,导致1,25-二羟基维生素D的降解3为了减弱生物利用度和预防高钙血症。考虑到这种调节,为什么即使补充维生素D,结石形成剂也会升高骨化三醇水平?
已经提出了各种机制来回答这样的一个问题,最近的证据说明答案可能与CYP24A1的突变有关,导致没办法使骨化三醇失活(图1),这在特发性婴儿高钙血症中得到了证明。10Schlingmann等人证明,在特发性婴幼儿高钙血症患儿中,在血清PTH抑制和1,25-二羟基维生素D非常明显升高的情况下,可见明显的肾钙质沉着和高钙血症。3由于CYP24A1突变。这些突变也在维生素D推注后遭受严重高钙血症的第二组队列中被发现。10正如预期的那样,CYP24A1敲除小鼠在外源性维生素D给药后显示高钙血症和肾钙质沉着症。13虽然在钙结石形成剂中已经发现了CYP24A1突变,但确切的患病率尚不清楚。这些个体可通过低 PTH 水平和骨化三醇值升高来与特发性结石形成剂区分开来。24,25-二羟基维生素D水平降低。
精准医学使基因检测更容易获得,成本更低,具有潜在的宝石病适用性。已经确定了特发性肾结石的多种潜在临床相关单基因病因。通过基因分型进行增强诊断是可行的,并已被建议用于诊断和治疗目的。14CYP24A1突变的杂合性可能易导致结石形成;因此,在用结石形成剂中补充维生素D之前,应考虑使用25(OH)D血清水平(高)和24,25(OH)维生素D水平(低)进行筛查,以避免钙尿症恶化。需要筛查和基因检测的患者是血清钙水平正常至高水平且 PTH 水平受抑制的患者。
其他遗传途径能更加进一步了解维生素D和尿石症的钙易感性。维生素 D 受体(VDR) 多态性可能会导致过度反应,导致尿钙排泄量增加,并且 sib-pair 连锁研究之后发现,特发性结石形成剂中的维生素 D 等位基因变异。15试图鉴定结石成形剂中VDR单核苷酸多态性的研究产生了不同的结果。16研究与性别、种族、紫外线照射和生活方式等变量之间的异质性是显著的局限性。另一个与钙结石形成易感性有关的候选基因是由CASR编码的钙感知受体CaSR。这些受于肾脏和甲状旁腺中,对钙化和磷酸钙沉淀具有保护作用。表达的改变会改变水、钙和磷酸盐之间的正常稳态。17该基因的启动子含有对VDR有反应的元素,钙感应受体激动剂能抑制由维生素D引起的动脉钙化。17虽然最近的全基因组关联研究已经确定了4个新的易感肾结石位点,但要进一步的研究来阐明遗传易感性肾结石的机制。18尽管进行了广泛的研究,但负责结石形成遗传力的确切基因仍然难以捉摸。
遗传性高钙结石形成(GHS)大鼠被选择性地繁殖以最大化尿钙排泄,是研究肾结石遗传学和病理生理学的理想选择。19GHS大鼠在标准饮食中排泄高达10倍的尿钙,并在将羟脯氨酸(草酸盐前体)添加到其饮食中时产生磷酸钙结石或草酸钙结石。20原则上,其机制似乎是由VDR数量增加介导的钙的肠道吸收。19GHS大鼠在骨骼和肾脏中的VDR也增加,涉及骨骼再吸收,以及在岩性发生中未能再吸收过滤的钙。20当给予骨化三醇时,与对照组相比,骨吸收和尿钙显着增加。给予骨化三醇前体胆钙化醇,在这些大鼠中产生肾结石,尽管口服钙没有。21GHS大鼠反映了特发性结石形成者的常见代谢异常,尽管遗传图谱仍然不完整,但它们进一步了解使人类易患岩成性的复杂多遗传学。
最终升高的骨化三醇水平会增加钙质和肾结石。11然而循环25-羟基维生素D的关系3(骨化三醇的直接前体)到肾结石的形成不太清楚,可以说更重要,因为它是维生素D状态的公认临床测量。荟萃分析显示,关于 25-羟基维生素 D 的结果好坏参半3与成岩风险相关的水平。22循环 25-羟基维生素 D 升高3和1,25二羟基维生素D3在高钙化剂中发现,但未见正常钙化结石形成剂。一些纳入的研究表明,1,25二羟基维生素D升高3在正常钙质结石形成者与对照组之间,但无统计学差别。22多种遗传多态性和生活方式差异的作用可能代表了上述数据中未控制的变量。这些维生素D代谢物缺乏一致的作用凸显了钙稳态和结石形成的复杂性,要进一步研究以确定可能面临补充风险的表型亚组。
在迄今为止关于维生素D和肾结石的最大研究中,研究了3个特征良好的队列:卫生专业技术人员随访研究中的男性和护士健康研究中的女性I和II。6在近200,000名长期前瞻性随访的男性和女性中,在多变量调整后未发现维生素D摄入量与结石风险之间有关联。护士健康研究II组有一个高风险的建议,P值为0.02;但是,置信区间包括 1.0。6这些人补充维生素D的适应症尚不清楚,队列中很少有人每天摄入的维生素D超过2000 IU;作者得出结论,在“典型量”中,维生素D与肾结石之间没有关联。6先前的研究在很大程度上是一致的,包括先前对卫生专业技术人员随访研究的分析。23这一发现在2000多名患者中得到了证实,表明25-羟基维生素D升高之间没有关联。3和结石,与补充维生素 D 和结石风险无关,但随访时间短且结石发病率低。24
大多数介入研究和荟萃分析都混淆了维生素 D 作为伴随钙补充剂在结石形成中的致病因素的真正作用。虽然膳食钙与钙结石形成呈负相关,但非食物性钙补充剂与结石呈正相关。维生素D与钙补充剂增加高钙尿大鼠的结石。美国预防服务工作组(USPSTF)发现足够的证据说明,补充维生素D和钙会增加肾结石的发病率。这一发现基于来自3项随机对照试验(n= 39,659)的证据,其中4-7年联合补充维生素D和钙会增加肾结石的发病率;合并的绝对风险差为0.33%(0.06%-0.60%),合并的RR为1.18(1.04-1.35)。在妇女健康倡议(WHI)中,服用400 IU维生素D和1000毫克元素钙的绝经后妇女肾结石的发病率增加(HR 1.17,95% CI 1.02-1.34)。虽然风险比不大,但大量女性服用补充剂使风险在临床上具备极其重大意义。26若使用柠檬酸钙而不是碳酸钙,是否会抑制岩性发生,或者随餐补时9与维生素D一起仍然是悬而未决的问题。有必要注意一下的是,Curhan等人发现每日补钙的使用与肾结石(保护性或别的方面)之间没有显着关联。作者还推测,这可能是由于补充的时间,因为膳食钙抑制了岩性发生。2Malihi等人2019年的另一项最新研究表明,高剂量补充维生素D(不含钙)不会增加结石形成或血清钙的风险,中位随访时间超过3年。29
尽管 WHI 结果为,血清 25(OH)D 与 400 IU 的边际预期增加不太可能会引起高钙血症(以及随后的尿钙增加),特别是考虑到该队列中相比来说较低的基线
在已知的维生素D缺乏症结石形成剂中,Leaf等人发现补充维生素D并未显着增加平均尿钙排泄。一些患者增加,而另一些患者则减少,这表明维生素D补充最好通过24小时尿液收集来监测。30Jorhi等人确实注意到补充维生素D的结石形成者中24小时尿钙的增加,尽管没有统计学意义(P= .06),但26名从“正常”钙排泄开始的患者中有6名过渡到显着更高的水平。31这些例外可能是前面提到的具有CYP24A1或VDR多态性的群体吗?作者建议同样多,但在两项研究中都没有对CYP24A1或其他突变做评估。尽管这两项研究在维生素 D 的配方和维持的时间上存在一定的差异,但可以合理地得出结论,补充维生素 D 监测成石剂中尿钙排泄可能是合适的。31
低水平的25-(OH)D与许多不良事件有关,包括骨折,跌倒,心血管疾病,结直肠癌,糖尿病,抑郁症,认知能力变弱和死亡。32补充维生素D的随机试验通常不支持这些关联作为因果关系。关于骨骼健康,对无症状维生素D缺乏人群补充剂的荟萃分析发现,平均跌倒次数减少,但骨折没有减少;发现死亡风险降低,但在排除老年机构妇女试验时,死亡风险没有持续。32WHI研究确实发现,在无症状的患者中,补充BMD的小幅增加,但骨折没有减少。27因此,美国预防服务工作组发现只有少数的证据建议对男性和绝经前妇女进行筛查,并建议不要每天补充400 IU或更少的维生素D和1000毫克或更少的钙,以预防社区居住的绝经后妇女骨折。28Hansen等人在一项针对25-(OH)D水平低于30 ng / mL的绝经后妇女的随机对照试验中显示,安慰剂,低剂量或高剂量胆钙化醇在BMD,肌肉功能,肌肉质量或跌倒方面没有差异。33最近,卡尔加里大学2019年的一项随机对照试验对健康成年人进行了为期3年的随访,并证明放射状和胫骨的BMD降低,使用400 IU作为参考点,维生素D剂量大幅度的增加。34
从历史上看,维生素D测定是在代谢骨骼健康中确定的作用。然而,维生素D的可能(并且广为人知)的非骨骼益处引起了人们对其多效性,非骨骼作用的兴趣。35观察性研究表明,25-(OH)D与多种疾病之间有负相关关系,因此近年来全世界范围内的检测和补充剂显着增加。7在无症状的初级预防环境中,补充维生素D对心血管疾病或癌症没有益处。36此外,最近对34项介入性研究进行的一项大型系统评价显示,补充维生素D没有带来非骨骼益处,尽管老年妇女的全因死亡率略有降低。37虽然争议尚未解决,但事实上,补充补充剂的好处在无数的研究中得到证实,这使得低水平的25-(OH)D可能是健康情况不佳的结果,而不是原因。
为了应对持续不断的发展的数据,已经尝试遏制测试。美国临床病理学会发起了“明智地选择”倡议,建议不要对25-(OH)D进行基于人群的筛查,因为他们确定该测试没有益处。38此外,Manson等人指出,维生素D水平的临床和研究应用在很大程度上是基于对参考值的误解和误用,并且对维生素D缺乏“大流行”的担忧是没有根据的。39推荐的20 ng / mL骨骼健康膳食津贴通常被用作“切口点”,而实际上它是需求范围的上限,并且大多数(97.5%)的人口有这种或更少的要求。因此,在无症状患者中进行常规筛查和补充可能没什么益处,并且可能对某些遗传易感结石形成剂产生理论上的危害。
患有非创伤性骨折,肝或肾功能障碍或吸收不良疾病的有症状人群显然需要对骨骼健康进行干预,结石形成者也不例外。事实上,肾结石病史和尿钙排泄率较高易导致BMD降低3并且与男性和女性手腕骨折的风险较高独立相关。此外,在泌尿石症患者中,维生素 D水平不足的患病率超过 80%,并且与结石检查时的代谢异常相关,这使得该人群特别容易建议补充。8那么如何治疗有骨质减少或骨质疏松症的高危结石?CYP24A1突变的筛查是可用的,并且可能具有效用;然而,有替代药理学能增加BMD,同时增加结石预防的益处,甚至已经根据经验建议用于高危结石形成剂。41
噻嗪类药物已被美国泌尿外科协会和欧洲泌尿外科协会推荐用于钙结石预防,meta 分析显示的相对复发风险降低了 47%。42噻嗪类药物直接增加远端肾小管中的钙吸收,间接增加近端肾小管中的钙吸收,由此减少钙尿。因此,保留钙使男性的BMD在脊柱和髋关节的年率分别增加8%和3%。43这些结果在一项基于人群的大型病例对照研究中得到了证实,该研究针对丹麦接受高血压治疗的40,000多名患者进行了研究。作者报告称,在调整混杂因素后,目前使用噻嗪类药物可使前臂骨折减少 17%,任何骨折减少 10%。Pak等人在脊柱,股骨颈和桡骨轴密度方面表现出与噻嗪类和柠檬酸钾相似的改善,导致结石形成基本上完全停止。噻嗪类药物有低钾血症的风险,因此建议补充低枸橼酸钾。
低枸橼尿症在成石剂中极为常见,枸橼酸钾通过增加尿枸橼酸盐和减少钙排泄来独立地减少肾结石复发。慢性酸负荷是高蛋白饮食的常见后果,不仅与岩性发生有关,23但骨量也减少。46Jehle 等人在一项针对绝经后骨质减女的随机前瞻性对照试验中,证明了柠檬酸钾在减少尿钙、增加尿枸橼酸盐和明显地增加骨量方面的疗效。46据推测,这些影响是通过中和膳食质子和减少尿钙排泄而发生的。同一组在骨质疏松性老年患者中给予柠檬酸钾24个月,改善了骨微结构。副作用包括胃肠道不适和腹泻。如果担心高钾血症,则可考虑使用柠檬酸钠。然而,这不会减少尿钙的排泄,并可能增加结石的形成。
骨骼健康的首选疗法是给予双膦酸盐。这是一类成熟的骨质疏松症治疗方法,可有效抑制骨吸收。48在一项随机对照试验中,Giusti 等人发现,骨质疏松症中 BMD 有所改善,24 小时尿钙与阿仑膦酸盐一起降低,尿钙排泄量增加。同时使用噻嗪类药物对骨骼健康和尿钙的益处显着增加。49双膦酸盐在前瞻性随访队列中的成石剂中产生了相同的结果,同时抑制了成石活性。50Weisinger等人在18种高钙结石形成剂中使用双膦酸盐可减少24小时尿钙排泄,同时骨更新减少和腰椎BMD增加。正常钙质对照组未发现尿钙减少,这表明骨吸收在岩性发生中起作用。51对双膦酸盐的广泛研究表明它们拥有非常良好的耐受性和安全性;然而,尽管有数据,但它们的使用存在显着的阻力。已经观察到无数的不良事件,包括胃肠道不耐受,非典型股骨骨折和颌骨坏死(ONJ);然而,这些都是罕见的,并且难以复制。52ONJ受到关切,尽管在病例报告和系列报告中有所发现,但没有因果前瞻性研究。ONJ最常出现在晚期癌症和多发性骨髓瘤中使用的较高剂量,每患者年暴露的发生率低于1/100,000。最后,唑来膦酸预防骨折的显着作用也在骨质减少的女性中得到了证明;人们会期望在骨质功能不全的女性中降低尿钙和产石益处,这是一个更容易骨折的群体。
肾结石对生命和生活品质有重大影响。与肥胖和饮食有关的患病率是无可争议的。广泛筛查维生素 D导致补充维生素 D 似乎无助于一般人群在治疗剂量下出现肾结石风险。在已知的结石形成剂中,骨化三醇升高确实会增加产石风险,维生素 D 可能会增加CYP24A1突变患者的结石。基因检测虽然可能有助于预防,但对世界大部分人口来说却不是可用的,也不是必需的。维生素D对没有佝偻病风险的成年人的益处的证据很少,优越的药理学能增加BMD,同时减少结石,副作用最小且可控。